Problemas del primer principio de la termodinámica (GIE)
De Laplace
1 Trabajo en una compresión isoterma por un peso
Un cilindro vertical de 10.0 cm de diámetro contiene hidrógeno a 25°C y 100 kPa de presión, que también es la temperatura y presión exterior. La tapa del cilindro puede deslizarse sin rozamiento e inicialmente se encuentra a 10.0 cm de altura. Suponga que las paredes y el émbolo son superficies diatérmicas.
- Se coloca sobre la tapa una pesa de 2.0 kg. Calcule el trabajo realizado sobre el sistema desde el momento que se coloca la pesa hasta el estado de equilibrio final.
- Suponga que en lugar de una pesa se colocan sobre lentamente el émbolo 2.0 kg de arena grano a grano. ¿Cuál es en ese caso el trabajo realizado sobre el sistema?
Para los dos casos anteriores, halle la variación en la energía interna del gas y el calor que entra en el sistema durante el proceso.
2 Sucesión de tres procesos cuasiestáticos
Un cilindro de 20 cm de diámetro contiene aire y está cerrado por un émbolo. Inicialmente el aire tiene una temperatura de 27 °C y una presión de 100 kPa, que también es la presión exterior, estando el émbolo a 10 cm del fondo. Entonces se realiza el siguiente proceso cuasiestático
- I: Se atornilla el émbolo y se calienta el aire hasta 327 °C, sumergiéndolo en un baño a esta temperatura.
- II: Se libera el émbolo lentamente, dejando que se expanda el aire hasta que su presión vuelve a ser la inicial. En este proceso el aire se mantiene a la temperatura de 327 °C.
- III: Con el émbolo libre, se enfría gradualmente hasta que la temperatura vuelve a ser la inicial.
Para este proceso:
- Halle la presión, volumen y temperatura al final de cada fase del proceso.
- Calcule el trabajo en cada fase, así como el trabajo neto total.
- Calcule la variación en la energía interna y el calor en cada paso y su variación neta.
3 Mezcla de dos cantidades de agua
Se ponen en contacto 750 cm³ de agua a 20 °C con 250 cm³ de agua a 80 °C. ¿Cuál es la temperatura final de la mezcla? ¿Cuánto calor ha pasado de un subsistema al otro?
4 Mezcla de agua e hielo
Dentro de un recipiente adiabático se sumerge un bloque de 100 g de hielo a 0.0 °C en 1.0 litros de agua a 20 °C. Determine si se funde todo el hielo y la temperatura final del sistema. ¿Qué ocurre si en lugar de 100 g se tiene 1.0 kg de hielo?
5 Calor necesario para evaporar hielo
Calcule la cantidad de calor necesaria para llevar un bloque de hielo de 500 g inicialmente a −10 °C hasta el estado de vapor de agua a 115 °C, manteniéndose la presión constante en 101.3 kPa.
6 Mezcla de hielo y vapor de agua
En un recipiente a presión constante de 101.3 kPa, se ponen en contacto 1.0 m³ de vapor de agua a 115 °C con 500 g de hielo a −10 °C. Determine la temperatura final del sistema.
7 Calentamiento de un gas a volumen y a presión constante
Un cilindro de 20 cm de diámetro está cerrado por un émbolo. La presión exterior es en todo momento de 100 kPa. La cámara está llena de aire que se encuentra inicialmente a 300 K y el émbolo está a una distancia de 10 cm respecto del fondo. Se calienta cuasiestáticamente el gas hasta que su temperatura llega a 450 K. Calcule el calor que entra el gas, el trabajo que se realiza sobre él, así como la variación de su energía interna y de su entalpía:
- Si el émbolo está bloqueado de forma que no puede desplazarse.
- Si el émbolo está libre y puede deslizarse sin rozamiento por el tubo.
8 Calentamiento de agua con una resistencia
En una cámara con un émbolo móvil se coloca 500 cm³ de agua a 300 K. El exterior se encuentra a una presión de 100 kPa. Se le comunica lentamente calor al agua hasta que se evapora por completo.
- Calcule el calor necesario para que se realice este proceso.
- Halle el trabajo que se realiza sobre el agua.
- Calcule la variación en la entalpía y en la energía interna del agua.
- Suponga que el calentamiento se produce mediante una resistencia eléctrica a una tensión de 220 V por la que pasa una corriente de 2 A. ¿Cuánto tiempo tarda en realizarse el proceso? En este caso, la energía entra en el sistema en forma de calor o de trabajo?
9 Compresión adiabática de un gas por un peso
Un cilindro vertical de 10.0 cm de diámetro contiene hidrógeno a 25 °C y 100 kPa de presión, que también es la temperatura y presión exterior. La tapa del cilindro puede deslizarse sin rozamiento e inicialmente se encuentra a 10.0 cm de altura. Suponga que las paredes y el émbolo son superficies adiabáticas.
- Se coloca sobre la tapa una pesa de 2.0 kg. Calcule el trabajo realizado sobre el sistema desde el momento que se coloca la pesa hasta el estado de equilibrio final.
- Suponga que en lugar de una pesa se colocan sobre lentamente el émbolo 2.0 kg de arena grano a grano. ¿Cuál es en ese caso el trabajo realizado sobre el sistema?
Para los dos casos anteriores, halle la variación en la energía interna del gas y el calor que entra en el sistema durante el proceso.
10 Compresión lineal de un gas
Se tiene un volumen V0 de un gas ideal diatómico a una presión p0 y una temperatura T0 encerrado en un recipiente con un pistón móvil. Este gas se comprime reversiblemente según la ley
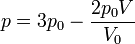
reduciéndose el volumen hasta V0 / 2.
- Trace la gráfica del proceso en un diagrama pV.
- Calcule la temperatura final del proceso.
- Calcule el trabajo neto realizado sobre el gas, la variación de su energía interna y el calor que entra en el gas durante el proceso.
- ¿Para qué volumen durante el proceso la temperatura es máxima? Halle el valor de esta temperatura máxima.
- Separando el proceso en dos: uno hasta que alcanza la temperatura máxima y otro de ahí hasta el final, halle W, ΔU y Q en cada uno de los dos subprocesos.
11 Expansión lineal de un gas
Se tiene una cantidad fija de un gas ideal diatómico situada a una presión p0, volumen V0 y temperatura T0. Experimenta un proceso tal que la presión final es 2p0 y el volumen 2V0.
- En este proceso, ¿cómo varía la temperatura?
- Halle el incremento de la energía interna en este proceso
Supongamos que el proceso anterior ocurre de manera cuasiestática según la ley
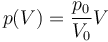
- ¿Cuánto trabajo se realiza sobre el gas en esta expansión cuasiestática?
- ¿Cuánto calor entra en el gas en la expansión cuasiestática?
12 Termómetro de gas
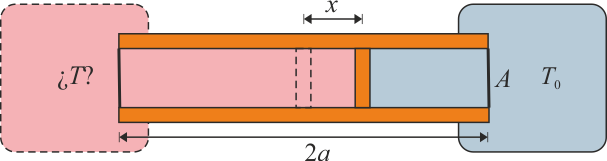
Se construye un termómetro de gas ideal según el siguiente principio: un tubo cilíndrico de sección S y longitud 2a con paredes adiabáticas y bases diatermas es dividido por un pistón, también adiabático, que puede deslizarse sin rozamiento por el interior del tubo. En el interior de las dos cámaras se encuentra un gas ideal. Una de las dos cámaras se mantiene en contacto térmico con un foco a temperatura T0, mientras que la otra se pone en contacto con el sistema cuya temperatura se quiere medir. Cuando las dos temperaturas son iguales el pistón se encuentra en la posición central y la presión del gas es p0.
- Calcule la temperatura absoluta T a la que se encuentra el sistema cuando el pistón se ha desplazado una cantidad x desde el centro hacia el sistema a T0. ¿Resulta una escala lineal de temperaturas? ¿A cuánto tiende x si
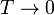 o si
o si 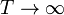 ?
?
- Supongamos que se parte del equilibrio a T0 y que la variación de la temperatura del gas de la cámara exterior y el desplazamiento del pistón en x ha sido de forma cuasiestática y reversible. ¿Cuáles son los calores, trabajos e incrementos de energía interna para cada una de las cámaras y para el tubo completo, como función del desplazamiento x del pistón?
- Supongamos que el tubo mide 20 cm, la temperatura de referencia es
 y el pistón se desplaza 1 cm. ¿Cuál es la temperatura del sistema exterior?
y el pistón se desplaza 1 cm. ¿Cuál es la temperatura del sistema exterior?
- Si además sabemos que la sección del tubo es de 10 cm², el gas contenido es aire y la presión inicial es
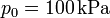 , ¿cuánto valen los calores, trabajos e incrementos de energía interna del segundo apartado?
, ¿cuánto valen los calores, trabajos e incrementos de energía interna del segundo apartado?
13 Calor que escapa por una ventana
En una habitación que se encuentra a una temperatura de 22 °C se encuentra una ventana de 1.60 m por 1.20 m. con un vidrio de 5 mm de espesor. El exterior de la habitación se halla a 10 °C. Determine aproximadamente la cantidad de calor que escapa de la habitación por segundo. La conductividad térmica del vidrio es de 0.96 W/m·K.
Suponga ahora que delante de la ventana se colocan unos finos visillos de espesor despreciable, estando los visillos a 2 cm de la ventana. ¿Cuál es entonces la cantidad de calor que escapa de la ventana por segundo? La conductividad térmica del aire vale 0.024 W/m·K
14 Calor que escapa del cuerpo humano
Determine la cantidad de calor que escapa por cm² de piel del cuerpo humano si la piel se encuentra a 33 °C y el aire exterior se encuentra a 15 °C, estando el cuerpo cubierto por una sábana de algodón de 1 mm de espesor. ¿Y si además de la sábana está tapado con una manta de lana de 5 mm de espesor? La conductividad térmica de la lana es 0.03 W/m·K y la del algodón 0.04 W/m·K.
15 Congelamiento gradual de un estanque
Un estanque de agua a 0 °C está cubierto por una capa de hielo de 4.00 cm de espesor. Si la temperatura del aire permanece constante a -10.0 °C, ¿cuánto tardará el espesor de la capa de hielo en alcanzar los 8.00 cm?
La conductividad térmica del hielo es 2.22 W/m·K y la entalpía de fusión del agua vale 334 kJ/kg.
16 Trabajo en un gas con resorte
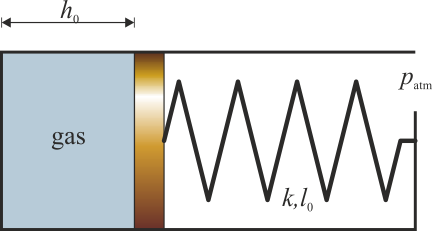
Se tiene un cilindro de sección S en el interior del cual hay un pistón que puede deslizarse sin rozamiento. El pistón cierra una cámara en la que hay un gas ideal. La cara exterior del pistón está unida al extremo del tubo mediante un resorte de constante k y longitud natural l0. Esta parte del tubo está abierta a la atmósfera. Para un cierto valor de la temperatura, T0, la presión es la atmosférica, el pistón se encuentra a una distancia h0 del fondo y el resorte no ejerce fuerza alguna. Cuando el gas se calienta, se expande y el resorte se comprime.
- Halle el trabajo realizado sobre el gas cuando su temperatura pasa de T0 a T1.
- Calcule la variación de la energía interna del gas y el calor transferido al gas en el proceso.
- Calcule el trabajo, la variación en la energía total y el calor, si consideramos que el sistema esta formado por el gas y el muelle.
17 Fusión de un trozo de hielo
Se tiene un bloque de hielo de masa 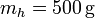 sumergido en un volumen de agua de masa
sumergido en un volumen de agua de masa 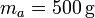 , ambos a una temperatura
, ambos a una temperatura 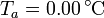 . El conjunto está contenido en un recipiente cilíndrico
de vidrio, de diámetro
. El conjunto está contenido en un recipiente cilíndrico
de vidrio, de diámetro 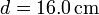 y espesor
y espesor 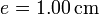 , abierto por arriba al aire (que se puede suponer un aislante térmico perfecto). El recipiente está sumergido en un baño de agua a
, abierto por arriba al aire (que se puede suponer un aislante térmico perfecto). El recipiente está sumergido en un baño de agua a 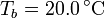 .
.
- Calcule la superficie de agua en contacto con el recipiente y la cantidad de calor que entra en él en 1.00 s.
- Halle la cantidad de hielo que se funde en el mismo tiempo. ¿Cuánto tiempo tardará aproximadamente en derretirse por completo?
Datos: Densidad de masa del agua líquida 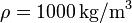 ; Conductividad térmica del vidrio
; Conductividad térmica del vidrio 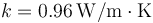 ; Entalpía específica de fusión:
; Entalpía específica de fusión: 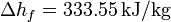 .
.





