Mezcla de dos cantidades de agua
De Laplace
Contenido |
1 Enunciado
En un recipiente adiabático se ponen en contacto 750 cm³ de agua a 20°C con 250 cm³ de agua a 80°C, siendo la temperatura exterior de 50°C. ¿Cuál es la temperatura final de la mezcla? ¿Cuánto calor entra en cada subsistema?
¿Cómo cambian los resultados si las paredes son diatermas?
¿Cuánta entropía se produce en el proceso, en cada uno de los casos?
2 Paredes adiabáticas
En el primer caso, el recipiente está aislado térmicamente del exterior, por lo que la temperatura del ambiente es irrelevante. Tenemos un sistema aislado formado por las dos masas de agua. El único calor fluye de una parte del agua a la otra, pero no con el exterior. Si llamamos “1” al agua caliente originalmente y “2” a la fría, os queda la relación
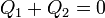
o, dicho de otra forma
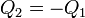
el calor que entra en el agua fría es igual al que sale de la caliente. Podemos escribir esto como
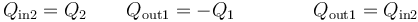
Por otro lado, el calor que entra en el agua fría es proporcional a la diferencia de temperaturas entre la final y la inicial
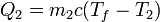
y el calor que entra en el agua caliente (que tendrá un valor negativo, porque en realidad sale) cumple la misma ley
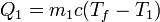
El calor específico del agua, c, depende poco de la temperatura, por lo que podemos suponer el mismo valor para las dos masas de agua.
Llevando esto al calor neto
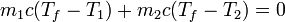
y despejando obtenemos la temperatura final
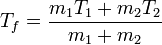
Puesto que a este resultado se llega a partir de diferencias entre temperaturas es válido tanto para temperaturas expresadas en grados Celsius como en kelvins.
Para sustituir los valores numéricos observamos que se nos dan los volúmenes, no las masas. Sin embargo, puede suponerse que dentro del rango de temperaturas la densidad del agua permanece constante, por lo que
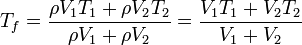
es decir, también se trata de la media ponderada respecto a los volúmenes. 3/4 l de agua cuentan el triple que 1/4 l. Sustituyendo los valores numéricos en grados Celsius
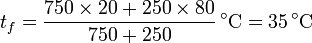
La cantidad de calor que va del agua caliente a la fría es
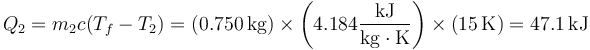
Al mismo resultado se llega, por supuesto, si en lugar del calor que entra en el medio 2, hallamos el que sale del medio 1
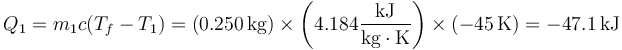
Gráficamente, tendríamos una representación como la de la figura
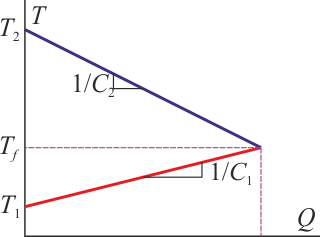
la parte 1, que tiene más masa, posee una mayor capacidad calorífica, por lo que el aumento de temperatura, para una cantidad de calor dada, es menor que el descenso en la temperatura de la parte 2, que por ser más ligera tiene menos capacidad calorífica. La temperatura de equilibrio lo da el corte de las dos rectas y la cantidad de calor intercambiada es la abscisa de la gráfica.
3 Paredes diatermas
En el segundo caso, el sistema alcanza finalmente el estado de equilibrio térmico con el ambiente, por lo que la temperatura final de cada parte de agua es la misma que la exterior
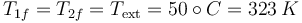
La cantidad de calor que entra en en el agua caliente es
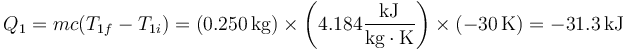
Es negativo porque en realidad sale. Para el agua fría
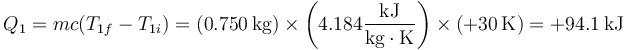
La cantidad neta de calor que entra en el sistema en este caso no es nula
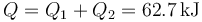
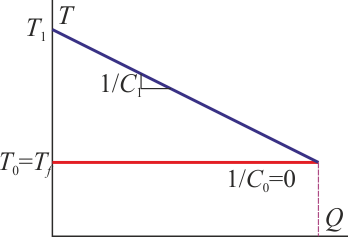
En este caso la gráfica seria la correspondiente a que haya presente un foco térmico, cuya temperatura es constante
4 Producción de entropía
4.1 Paredes adiabáticas
Para hallar la variación de la entropía del sistema debemos considerar un proceso reversible que lleve del estado inicial al final para cada una de las dos masas de agua.
La forma de hacerlo es considerar cada parte por separado y suponer que el calor que entra en cada una no procede de la otra, sino de una serie de focos térmicos situados a las temperaturas intermedias, de forma que imaginamos que el agua fría se va calentando gradualmente porque van entrando cantidades diferenciales de calor, de forma que la variación en su entropía es
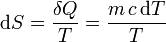
E integrando esta expresión
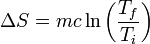
Esto nos da, para el agua inicialmente caliente
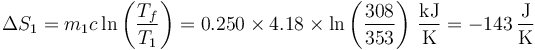
y para el agua inicialmente fría
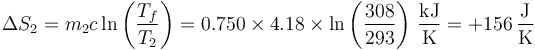
siendo la producción total de entropía
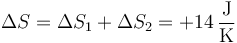
Esta cantidad es positiva, como corresponde a un proceso posible.
4.2 Paredes diatermas
Aplicando el mismo caso al caso de pareces diatermas, tenemos, para el agua inicialmente caliente
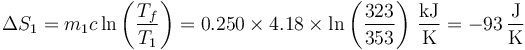
y para la inicialmente fría
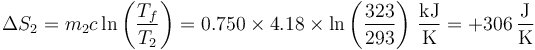
siendo la variación total de entropía del sistema
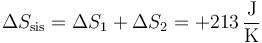
En este caso tenemos también variación de entropía del ambiente, ya que no es un proceso adiabático. Para el ambiente, el intercambio de calor es isotermo, ya que su temperatura es la misma en todo momento
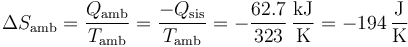
siendo la variación total de entropía del universo
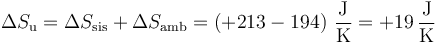
que de nuevo es positiva, como corresponde a otro proceso posible.





