Problemas de gases ideales en equilibrio (GIA)
De Laplace
(Diferencias entre revisiones)
(Página creada con '== Volumen y número de moléculas de un gas == Utilizando la ecuación de estado de los gases ideales, responde a las siguien…') |
(→Volumen y número de moléculas de un gas) |
||
| Línea 3: | Línea 3: | ||
#¿Qué volumen ocupa un mol de gas en condiciones estándar? | #¿Qué volumen ocupa un mol de gas en condiciones estándar? | ||
#¿Cuantas moléculas hay en <math>1.00\,\mathrm{cm^3}</math> de gas ideal a una temperatura de <math>300\,\mathrm{K}</math> y a un presión de <math>100\,\mathrm{kPa}</math>? ¿Y si la presión es de <math>1.00\times10^{-8}\,\mathrm{torr}</math>?. | #¿Cuantas moléculas hay en <math>1.00\,\mathrm{cm^3}</math> de gas ideal a una temperatura de <math>300\,\mathrm{K}</math> y a un presión de <math>100\,\mathrm{kPa}</math>? ¿Y si la presión es de <math>1.00\times10^{-8}\,\mathrm{torr}</math>?. | ||
| + | |||
| + | ==[[ Presión en un neumático GIA | Presión en un neumático ]]== | ||
| + | Un neumático de un automóvil se infla con aire que inicialmente se encuentra a una temperatura de 10.0<math>\,\mathrm{^oC}</math> y a presión atmosférica normal. Durante el proceso, el aire se comprime hasta alcanzar el 28.0% de su volumen original, lo que hace que aumente su temperatura a 40.0<math>\,\mathrm{^oC}</math> | ||
| + | #¿Cuál es la presión en el neumático? | ||
| + | #Después de hacer circular el coche a gran velocidad, la temperatura en el interior del neumático aumenta hasta 85.0<math>\,\mathrm{^oC}</math> y su volumen aumenta en un 2.00%. ¿Cuál es la nueva presión (absoluta) del neumático expresada en pascales? | ||
Revisión de 21:07 13 may 2013
1 Volumen y número de moléculas de un gas
Utilizando la ecuación de estado de los gases ideales, responde a las siguientes preguntas
- ¿Qué volumen ocupa un mol de gas en condiciones estándar?
- ¿Cuantas moléculas hay en
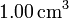 de gas ideal a una temperatura de
de gas ideal a una temperatura de 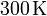 y a un presión de
y a un presión de 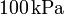 ? ¿Y si la presión es de
? ¿Y si la presión es de 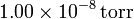 ?.
?.
2 Presión en un neumático
Un neumático de un automóvil se infla con aire que inicialmente se encuentra a una temperatura de 10.0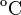 y a presión atmosférica normal. Durante el proceso, el aire se comprime hasta alcanzar el 28.0% de su volumen original, lo que hace que aumente su temperatura a 40.0
y a presión atmosférica normal. Durante el proceso, el aire se comprime hasta alcanzar el 28.0% de su volumen original, lo que hace que aumente su temperatura a 40.0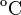
- ¿Cuál es la presión en el neumático?
- Después de hacer circular el coche a gran velocidad, la temperatura en el interior del neumático aumenta hasta 85.0
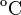 y su volumen aumenta en un 2.00%. ¿Cuál es la nueva presión (absoluta) del neumático expresada en pascales?
y su volumen aumenta en un 2.00%. ¿Cuál es la nueva presión (absoluta) del neumático expresada en pascales?





