Máquinas térmicas (GIE)
De Laplace
Contenido |
1 El primer principio en procesos cíclicos
2 Máquina térmica
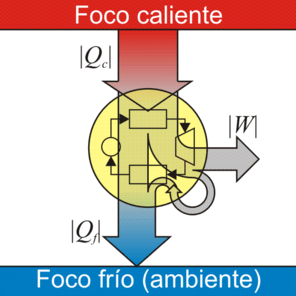
Una máquina térmica es un dispositivo que, operando de forma cíclica, toma de calor de un foco caliente, realiza un cierto trabajo (parte del cual se emplea en hacer funcionar la propia máquina) y entrega calor de desecho a un foco frío, normalmente el ambiente.2.1 Máquina de vapor
El ejemplo característico de máquina térmica es la máquina de vapor, que se emplea en la mayoría de las centrales eléctricas (sean estas térmicas, termo-solares o nucleares). En una máquina de vapor una cierta cantidad de líquido se hace hervir en un horno (foco caliente); el vapor resultante mueve una turbina, enfriándose parcialmente. El vapor enfriado pasa a un condensador, donde es enfriado a la temperatura ambiente, liberando calor y volviendo a ser líquido. Una bomba (movida por la turbina) toma ese líquido y vuelve a llevarlo al horno, manteniendo en marcha el sistema.
Tenemos cuatro términos energéticos en este proceso:
- El calor | Qc | proporcionado por el foco caliente.
- El calor | Qf | cedido al foco frío
- El trabajo | Wext | realizado por la turbina
- El trabajo Wint necesario para hacer funcionar la máquina térmica
La cantidad neta de trabajo que proporciona la máquina es lo que produce, menos lo que emplea en funcionar
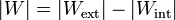
De acuerdo con el primer principio de la termodinámica, por tratarse de un proceso cíclico la energía interna del sistema no cambia en un ciclo, y el trabajo neto equivale a la diferencia entre el el calor que entra y el calor que sale
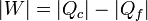
3 Rendimiento
Se define el rendimiento de una máquina térmica según el principio general de “lo que obtenemos dividido por lo que nos cuesta”. En este caso, “lo que obtenemos” es el trabajo neto. “Lo que nos cuesta” es el calor que entra procedente del horno. Por tanto
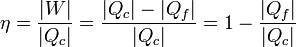
El funcionamiento de una máquina térmica se modela mediante un ciclo ideal en el cual una serie de procesos cuasiestáticos sustituyen a los procesos reales. Esta idealización permite el cálculo de parámetros del motor (como la presión o la temperatura máximas) que de otra forma sólo podrían determinarse empíricamente.
4 Ciclos termodinámicos
Entre los ciclos más importantes tenemos
- Ciclo Rankine, para máquinas de vapor.
- Ciclo Otto (GIE), que aproxima el comportamiento de los motores de explosión.
- Ciclo Diesel (GIE), para motores diésel.
- Ciclo Brayton (o Joule), que modela la conducta de una turbina de gas como las presentes en los motores de aviones.
Un ciclo ideal que sirve como referencia para el resto es el:
5 Máquinas reversibles
Una máquina reversible es una que puede operar en ambos sentidos, esto es, tanto como motor como como refrigerador. Esta máquina debe funcionar describiendo una serie de procesos cada uno de los cuales debe ser reversible (esto es, son procesos cuyo sentido de evolución se puede invertir mediante un cambio infinitesimal de las condiciones del entorno).
El concepto de máquina reversible, como el de proceso reversible, es una idealización. No existen máquinas reversibles en el mundo real, sino que deben considerarse como el límite al que tienden máquinas irreversibles cada vez más perfeccionadas.
El ejemplo más sencillo de máquina reversible es el de la máquina de Carnot, la cual opera según un ciclo de Carnot reversible. Cuando esta máquina se invierte se convierte en un refrigerador (o bomba de calor) de Carnot.
El rendimiento de una máquina reversible es
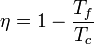
Cuando esta máquina funciona como refrigerador, su coeficiente de desempeño es
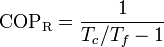
mientras que si actúa como bomba de calor será
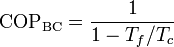
Entre los ciclos reversibles tenemos
5.1 Ciclo de Carnot
Para conseguir la máxima eficiencia la máquina térmica reversible que necesitamos debe tomar calor de un foco caliente, cuya temperatura es como máximo Tc y verter el calor de desecho en el foco frío, situado como mínimo a una temperatura Tf.
Para que el ciclo sea óptimo, todo el calor absorbido debería tomarse a la temperatura máxima, y todo el calor de desecho, cederse a la temperatura mínima. Por ello, el ciclo que estamos buscando debe incluir dos procesos isotermos, uno de absorción de calor a Tc y uno de cesión a Tf.
Para conectar esas dos isotermas (esto es, para calentar el sistema antes de la absorción y enfriarlo antes de la cesión), debemos incluir procesos que no supongan un intercambio de calor con el exterior (ya que todo el intercambio se produce en los procesos isotermos). La forma más sencilla de conseguir esto es mediante dos procesos adiabáticos reversibles (no es la única forma, el motor de Stirling utiliza otro método, la recirculación). Por tanto, nuestra máquina térmica debe constar de cuatro pasos:
- C→D Absorción de calor Qc en un proceso isotermo a temperatura Tc.
- D→A Enfriamiento adiabático hasta la temperatura del foco frío, Tf.
- A→B Cesión de calor | Qf | al foco frío a temperatura Tf.
- B→C Calentamiento adiabático desde la temperatura del foco frío, Tf a la temperatura del foco caliente, Tc.
Aplicando este resultado al caso de un gas ideal, se llega a que el rendimiento máximo de una máquina térmica es
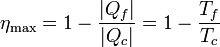
Para una máquina que trabaje entre 0°C y 100°C este rendimiento máximo es del 26.8%. ¡Muy lejos del 100% ideal!