Variación de entropía a volumen y presión constante
De Laplace
Revisión a fecha de 17:39 18 mar 2012; Antonio (Discusión | contribuciones)
Contenido |
1 Enunciado
Un cilindro de 20 cm de diámetro contiene aire inicialmente a 300 K, siendo la presión externa de 100 kPa. En el cilindro se encuentra un émbolo situado inicialmente a 15 cm de distancia del fondo. Se sumerge el cilindro en un baño térmico a 450 K. Calcule la variación de entropía del gas, del entorno y del universo si:
- El émbolo está atornillado en su posición.
- El émbolo puede deslizarse libremente.
2 A volumen constante
En el primer caso tenemos que el calor se le cede al gas, manteniendo éste constante su volumen.
El volumen inicial (y final del gas) vale

y el número de moles de gas es
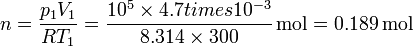
- Entropía del gas
- Hallamos la variación de la entropía a partir de la fórmula para un gas ideal en función de T y V (para aprovechar que V no cambia)
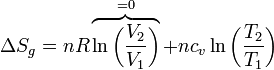
- Por comportarse el aire como un gas diatómico

- lo que da la variación de entropía
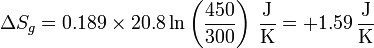
- Entropía del entorno
- Variación total





