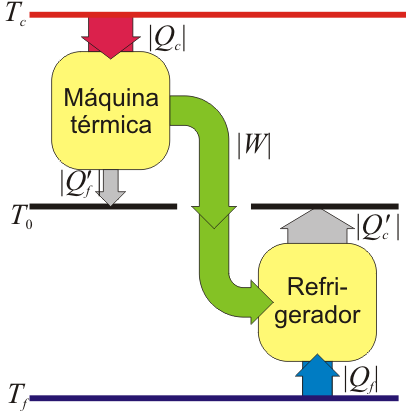
Refrigerador alimentado por una máquina térmica
De Laplace
Contenido |
1 Enunciado
(Final, Diciembre 2009, P2)
Un refrigerador que funciona entre una temperatura de -23 °C y la temperatura ambiente de 27 °C posee un coeficiente de desempeño de 3. Para hacer funcionar este refrigerador se emplea una máquina térmica que funciona entre 227 °C y la misma temperatura ambiente, la cual tiene un rendimiento de 0.2. Todo el trabajo producido por la máquina térmica se emplea en hacer funcionar el refrigerador.
- Definimos la eficiencia del conjunto máquina más refrigerador como el calor extraído del foco frío dividido por el calor que es necesario extraer del foco caliente, ¿cuál es la eficiencia del conjunto?
- Si se necesitan extraer 100 J por segundo del foco frío, ¿cuánto calor hay que extraer del foco caliente para hacer funcionar el sistema? ¿Cuánto trabajo realiza en la unidad de tiempo la máquina sobre el refrigerador?
- Calcule la producción de entropía en la unidad de tiempo debida a este conjunto.
- Si tanto el refrigerador como la máquina térmica fueran máquinas de Carnot, ¿cuál sería la eficiencia máxima del conjunto? ¿Qué calor sería necesario sacar del foco caliente en ese caso para extraer 100 J/s del foco frío?
2 Eficiencia del conjunto
Tenemos dos máquinas acopladas, cada una de las cuales opera entre temperaturas diferentes. Lo que tienen en común es que el trabajo que sale de una es el que entra en la otra.Tal como indica el enunciado, definimos el rendimiento de esta máquina como el cociente
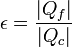
siendo | Qf | el calor que el refrigerador extrae del foco frío, y | Qc | el que la máquina toma del foco caliente. Ambas cantidades son proporcionales al trabajo común. Para el refrigerador
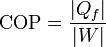
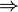 | Qf | = COP | W |
| Qf | = COP | W | y para la máquina
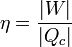
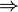
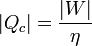
Dividiendo un calor por el otro
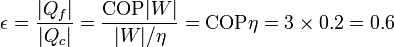
3 Calor y trabajo necesarios
Una vez que tenemos la eficiencia del conjunto, podemos hallar el calor necesario de forma inmediata
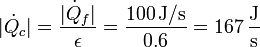
De forma parecida hallamos el trabajo intercambiado entre las máquinas
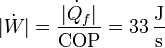
4 Producción de entropía
La producción de entropía se compone de cuatro términos, dos de los cuales son negativos, pues se extrae calor, y dos positivos, pues se vierte a él.
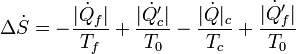
siendo 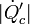 y
y 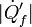 los calores cedidos al ambiente, en la unidad de tiempo, por el refrigerador y la máquina térmica respectivamente. Estos calores valen, para el del refrigerador,
los calores cedidos al ambiente, en la unidad de tiempo, por el refrigerador y la máquina térmica respectivamente. Estos calores valen, para el del refrigerador,
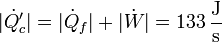
y para la máquina térmica
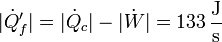
El hecho de que salgan iguales es puramente casual, consecuencia de los valores concretos de las eficiencias del refrigerador y la máquina.
Las temperaturas absolutas a las que se producen los intercambios son
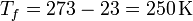
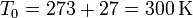
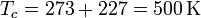
por lo que resulta la producción de entropía
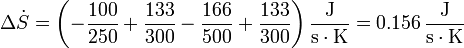
Esta producción de entropía es positiva, como corresponde a un proceso real.
5 Eficiencia máxima
La eficiencia máxima de un refrigerador la tiene uno sea una máquina de Carnot. El coeficiente de desempeño de este refrigerador es
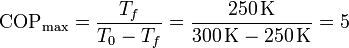
Una máquina térmica de Carnot posee la eficiencia máxima
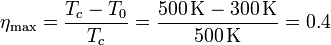
Un refrigerador de Carnot alimentado por una máquina también de Carnot poseerá también la eficiencia máxima
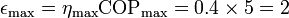
Como vemos, nuestro conjunto real tiene una eficiencia muy por debajo del máximo, por lo que es perfectamente posible.
Dado el rendimiento máximo, obtenemos el calor necesario para extraer 100 J/s del foco frío
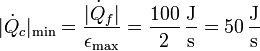
El trabajo necesario para extraer ese calor es ahora
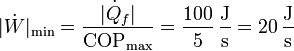
La producción de entropía en este caso es nula, por tratarse de un proceso completamente reversible.