Procesos de un gas ideal en diagramas GIA
De Laplace
Contenido |
1 Enunciado
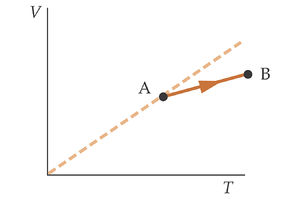
La figura de la izquierda muestra en un diagrama V-T un proceso realizado por una cantidad fija de un gas ideal. El gas pasa del estado A al estado B. ¿Qué ocurre con la presión del gas?
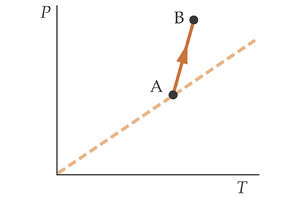
En la segunda gráfica tenemos otro proceso descrito por el gas en un diagrama P-T. ¿Qué ocurre en este caso con el volumen del gas?
2 Solución
2.1 Diagrama VT
Un gas ideal cumple la ecuación de estado
PV = nRT
En un diagrama VT, los procesos a presión constante vienen representados por rectas que pasan por el origen
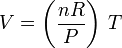
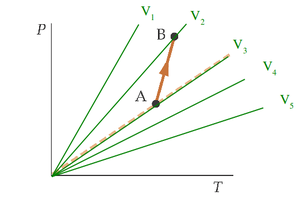
La pendiente de la recta es nR / P. Por tanto, es mayor cuanto menor es la presión. En la figura se representan varios procesos isóbaros. La relación entre las presiones es
P1 < P2 < P3 < P4 < P5
En el estado B la pendiente de la recta es menor que en el estado A . Por tanto su presión es mayor. Es decir
PB > PA
2.2 Diagrama PT
En un diagrama PT, los procesos a presión constante vienen representados por rectas que pasan por el origen
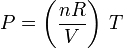
La pendiente de la recta es nR / V. Por tanto, es mayor cuanto menor es el volumen. En la figura se representan varios procesos isocóricos. La relación entre los volúmenes es
V1 < V2 < V3 < V4 < V5
En el estado B la pendiente de la recta es mayor que en el estado A . Por tanto su volumen es menor. Es decir
VB < VA