Dilatación y compresibilidad (GIE)
De Laplace
Contenido |
1 Introducción
En el caso de un gas podemos obtener, dentro de unos amplios límites de validez, una ecuación de estado que liga la presión, la temperatura y el volumen ocupado por el gas. Si éste es poco denso, esta ecuación es la del gas ideal
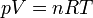
que también podemos escribir en la forma
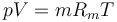
o, empleando la densidad de masa
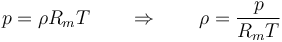
Esta ley nos da la densidad del gas ideal en función de la presión y la temperatura de cada estado.
Para un sólido o un líquido el comportamiento es mucho menos general. Una misma sustancia, como el agua, tiene conductas extremadamente variadas que impiden caracterizarla por una sola fórmula.
Por ello, solo podemos dar leyes locales, es decir, cómo varía la densidad cuando cambiamos un poco la temperatura y/o la presión alrededor de un estado dado. Matemáticamente, esto implica conocer las derivadas parciales

donde el subíndice indica qué magnitud permanece constante.
Es decir, la primera cantidad nos da cómo varía la densidad cuando cambia la temperatura, pero no la presión. Este fenómeno está asociado a la dilatación térmica.
La segunda derivada nos dice cómo cambia la densidad si aumentamos la presión manteniendo constante la temperatura. Esto está asociado a la compresibilidad.
En la práctica, estas cantidades también son empíricas. Manteniendo la presión constante se varía la temperatura y se mide como cambia la densidad. La derivada se halla mediante la aproximación
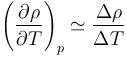
Veremos cada efecto por separado.
2 Dilatación
Una de las propiedades termométricas de uso más frecuente es la dilatación o contracción de una columna de un líquido (mercurio o alcohol) o de una fina tira metálica.
Estos termómetros se basan en el hecho empírico de que la longitud de una porción de material cambia con la temperatura (normalmente expandiéndose al aumentar ésta). La causa microscópica de este fenómeno es la variación de la energía cinética de los átomos del material, lo que provoca un cambio en las distancias de equilibrio entre los diferentes átomos, y que se traduce en una dilatación (o contracción) macroscópica.
2.1 Coeficiente de dilatación lineal
Considerando solo variables macroscópicas, la longitud de una porción de material será una función de la temperatura
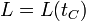
donde en general esta función podrá ser muy complicada.
Si consideramos pequeñas dilataciones de una pieza respecto a la longitud L0 que mide cuando la temperatura es t0, tenemos que en primera aproximación la dilatación de una pieza es proporcional a la propia longitud de la pieza, es decir, si una barra de 1 m se dilata 1 mm, una de 2 m se dilatará 2 mm. Por ello
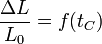
siendo f(tC) una cierta función de la temperatura, pero no de la longitud de la pieza. Esta función se anula en t0 y si nos separamos poco de esta temperatura podemos hacer una aproximación lineal y admitir que la dilatación es proporcional al incremento de temperatura (si con un incremento de 1°C se dilata 1 mm, con 2°C se dilata 2 mm), por lo que podemos escribir
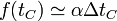
o, equivalentemente
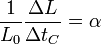
y

El factor α es el denominado coeficiente de dilatación lineal. Rigurosamente se define empleando derivadas en lugar de incrementos
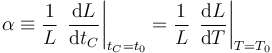
Las unidades en que se mide α en el SI son K − 1 (aunque, dado que se define a partir de incrementos, también pueden emplearse 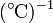 : normalmente es un valor muy pequeño, por lo que suelen usarse submúltiplos para expresarlo.
: normalmente es un valor muy pequeño, por lo que suelen usarse submúltiplos para expresarlo.
El coeficiente de dilatación lineal es una función de la temperatura, ya que se calcula a partir de la derivada en un cierto punto tC = t0. Si se halla a una temperatura diferente dará otro resultado (aunque si las temperaturas son próximas, los dos valores serán casi iguales).
Algunos valores de este coeficiente son
| Material | 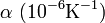 a 20°C | Material | 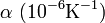 a 20°C | Material | 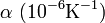 a 20°C | Material | 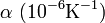 a 20°C |
|---|---|---|---|---|---|---|---|
| Aluminio | 23 | Agua | 69 | Acero inox. | 17.3 | Diamante | 1 |
| Etanol | 250 | Hierro | 11.8 | Hormigón | 12 | Mercurio | 61 |
| Oro | 14 | Plata | 18 | Vidrio | 8.5 | YbGaGe | ∼0 |
2.2 Coeficiente de dilatación superficial
El mismo principio se puede aplicar al área de una superficie sólida, que se dilata o contrae como consecuencia de la variación de la temperatura. Siguiendo el mismo razonamiento queda
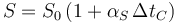
siendo αS el coeficiente de dilatación superficial, que se puede definir, para una temperatura fijada, como
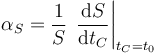
El coeficiente de dilatación superficial puede relacionarse con el dilatación lineal. Salvo en casos muy poco frecuentes, cuando una pieza de un material se dilata, todas sus dimensiones se multiplican en la misma proporción. Esto quiere decir que si tenemos una chapa metálica rectangular de base b0 y altura h0 a una temperatura t0, y la sometemos a un incremento de temperatura ΔtC, su nueva área será
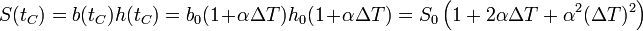
Puesto que las dilataciones son usualmente muy pequeñas el último término es despreciable, por lo que se puede hacer la aproximación
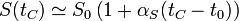
donde el coeficiente de dilatación superficial es igual al doble del lineal
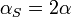
Hay que destacar que en una dilatación superficial (o volumétrica) todas las dimensiones se ven incrementadas. Esto quiere decir que si tenemos una pieza con un agujero, el tamaño del agujero aumenta con la temperatura, no se ve reducido porque el material rellene el agujero al dilatarse.
2.3 Coeficiente de dilatación volumétrico
De la misma manera que para una superficie, tenemos el aumento de volumen de un bloque como consecuencia del aumento de la temperatura
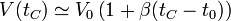
donde el coeficiente de dilatación volumétrico se define como
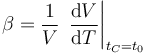
Para el caso de un sólido, empleando el mismo razonamiento que con el superficial, resulta un valor aproximadamente igual al triple del lineal
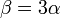
Esta relación puede comprobarse experimentalmente para multitud de materiales
No obstante, el coeficiente de dilatación volumétrico se aplica también a materiales que no sean sólidos, como líquidos y gases. Para estos no tiene mucho sentido hablar de dilatación lineal (pues su forma cambia, amoldándose al recipiente), pero la variación en el volumen es medible. Así, el agua a 20°C tiene un coeficiente de dilatación volumétrico de 2.07×10−4(°C)−1
2.4 Variación en la densidad
Si un bloque de un material se dilata su densidad disminuye, ya que la masa del bloque permanece constante. La variación de la densidad la obtenemos imponiento la conservación de la masa
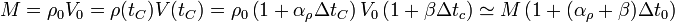
Puesto que la masa no varía con la temperatura, debe ser
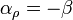
lo que nos da la disminución de la densidad
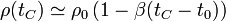
y una definición alternativa del coeficiente de dilatación volumétrico si lo que se conoce es la densidad como función de la temperatura:
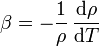
En general, la densidad depende de múltiples factores (presión, temperatura, etc.) por lo que es más riguroso emplear el símbolo de derivada parcial
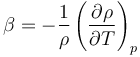
donde el subíndice p indica explícitamente que al calcular la derivada parcial la presión se mantiene constante.
2.5 Caso de un gas ideal
En el caso de un gas ideal es sencillo calcular el coeficiente de dilatación volumétrico. Para una presión dada el volumen es proporcional a la temperatura según la ley de Charles
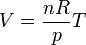
Derivando respecto a la temperatura y dividiendo por el propio volumen
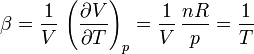
El símbolo de derivada parcial, y el subíndice p se incluyen para recordar que se trata de la derivada respecto a la temperatura, manteniendo constante la presión.
Para una temperatura de 25°C, este coeficiente de dilatación será igual
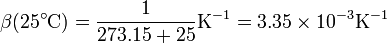
Esto quiere decir que si tenemos 1 l de gas a 25°C y subimos su temperatura 1°C (o 1 K) manteniendo constante su presión, el volumen aumenta en 3.35 cm³.
3 Compresibilidad
De manera análoga al coeficiente de dilatación se define el coeficiente de compresibilidad isoterma
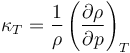
A diferencia del otro, este lleva un signo positivo ya que lo habitual es que la densidad aumente al comprimir una sustancia.
En el SI se mide en Pa-1.
Para la mayoría de líquidos y sólidos, este coeficiente es extremadamente pequeño. Así para el agua vale
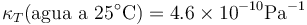
Esto quiere decir que para conseguir un aumento del 1% en la densidad del agua hace falta ejercer una presión
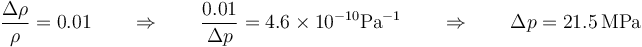
es decir, unas 200 atmósferas (lo que viene a ser sumergirse a 2000m de profundidad). Por esta razón puede suponerse habitualmente que el agua es incompresible, es decir, que su densidad no depende de la presión.
El hierro es aun más rígido que el agua. Para el hierro el coeficiente de compresibilidad vale 6×10−12Pa−1.
Además del coeficiente de compresibilidad, suele usarse el módulo de compresibilidad (bulk modulus en inglés), que se define como la inversa del otro
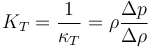
Este es un número muy grande, medido en pascales. Para el agua vale 2.15 GPa y para el hierro 170 GPa.
A pesar de la confusión entre nombres y símbolos, el coeficiente y el módulo de compresibilidad se distinguen fácilmente porque sus valores son muy diferentes.
Para un gas ideal puede calcularse teóricamente el coeficiente de compresibilidad
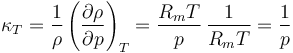
para la presión atmosférica, viene a valer 10−5Pa−1, que es un número pequeño, pero muy superior al del agua. Un gas ideal es unas 2000 veces más compresible que el agua.