Ciclo Otto
De Laplace
Contenido |
1 Enunciado
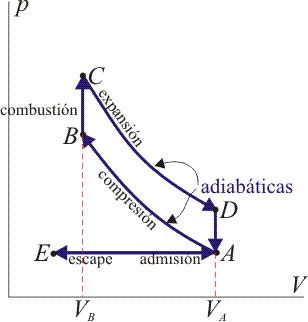
Un ciclo Otto ideal modela el comportamiento de un motor de explosión. Este ciclo está formado por seis pasos, según seindica en la figura. Pruebe que el rendimiento de este ciclo viene dado por la expresión
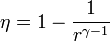
siendo r = V2 / V1 la razón de compresión. Para ello, halle el rendimiento a partir del calor que entra en el sistema y el que sale de él; exprese el resultado en términos de las temperaturas en los vértices del ciclo y, con ayuda de la ley de Poisson, relacione este resultado con los volúmenes V1 y V2.
2 Descripción del ciclo
Un ciclo Otto ideal es una aproximación teórica al comportamiento de un motor de explosión. Las fases de operación de este motor son las siguientes:- Admisión (1)
- El pistón baja con la válvula de admisión abierta, aumentando la cantidad de mezcla (aire + combustible) en la cámara. Esto se modela como una expansión a presión constante (ya que al estar la válvula abierta la presión es igual a la exterior.
- Compresión (2)
- El pistón sube comprimiendo la mezcla. Dada la velocidad del proceso se supone que la mezcla no tiene posibilidad de intercambiar calor con el ambiente, por lo que el proceso es adiabático. Se modela como una curva adiabática reversible, aunque en realidad no lo es por la presencia de factores irreversibles como la fricción.
- Explosión
- Con el pistón en su punto más alto, salta la chispa de la bujía. El calor generado en la combustión calienta bruscamente el aire, que incrementa su temperatura a volumen prácticamente constante (ya que al pistón no le ha dado tiempo a bajar).
- Expansión (3)
- La alta temperatura del gas empuja al pistón hacia abajo, realizando trabajo sobre él. De nuevo, por ser un proceso muy rápido se aproxima por una curva adiabática reversible.
- Escape (4)
- Se abre la válvula de escape y la subida del pistón empuja a los gases fuera de la cámara, con lo que se reduce el volumen de gas con una presión constante.
3 Eficiencia en función del calor
3.1 Trabajo y calor
Al analizar el ciclo Otto ideal, podemos despreciar en el balance los procesos de admisión y de escape a presión constante A→E y E→A, ya que al ser idénticos y reversibles, en sentido opuesto, todo el calor y el trabajo que se intercambien en uno de ellos, se cancela con un término opuesto en el otro.
De los cuatro procesos restantes, no se intercambia calor en los procesos adiabáticos, por definición. Sí se intercambia en los dos procesos isócoros.
- En la ignición de la mezcla, una cierta cantidad de calor Qc (procedente de la energía interna del combustible) se transfiere al aire.
- Al abrirse la válvula de escape y luego la de admisión, el aire (ya enfriado por la expansión) escapa y es sustituido por la misma cantidad de aire frío. Este proceso es equivalente a que la mezcla se enfríe, liberando una cantidad de calor | Qf | en el exterior