Enfriado de agua con hielo GIA
De Laplace
(Diferencias entre revisiones)
(Página creada con '==Enunciado== Para enfriar un litro de agua que está a 20°C se le añaden 250 gramos de hielo a -4°C. Determinar el estado final de la mezcla supuestas despreciables la…') |
(→Enunciado) |
||
| Línea 2: | Línea 2: | ||
Para enfriar un litro de agua que está a 20°C se le añaden 250 gramos de hielo a -4°C. Determinar el estado final de la mezcla supuestas despreciables las pérdidas de calor. | Para enfriar un litro de agua que está a 20°C se le añaden 250 gramos de hielo a -4°C. Determinar el estado final de la mezcla supuestas despreciables las pérdidas de calor. | ||
| - | Datos: calor específico del hielo, <math>c_h = 2.09\,\mathrm{kJ}/\mathrm{kg K} </math>; calor latente de fusión del hielo, <math>L_{fh}=334\,\mathrm{kJ}/\mathrm{kg}</math>. | + | Datos: calor específico del hielo, <math>c_h = 2.09\,\mathrm{kJ}/\mathrm{kg} \,\mathrm{K}\, </math>; calor latente de fusión del hielo, <math>L_{fh}=334\,\mathrm{kJ}/\mathrm{kg}</math>. |
[[Categoría:Problemas de Primer Principio F2 GIA]] | [[Categoría:Problemas de Primer Principio F2 GIA]] | ||
Revisión de 12:43 11 jun 2012
Enunciado
Para enfriar un litro de agua que está a 20°C se le añaden 250 gramos de hielo a -4°C. Determinar el estado final de la mezcla supuestas despreciables las pérdidas de calor.
Datos: calor específico del hielo, 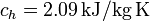 ; calor latente de fusión del hielo,
; calor latente de fusión del hielo, 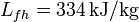 .
.





