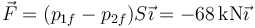Paso de calor entre dos cámaras rígidas
De Laplace
| Línea 32: | Línea 32: | ||
La cantidad de calor que pasa de una cámara a la otra es | La cantidad de calor que pasa de una cámara a la otra es | ||
| - | <center><math>Q_\mathrm{2in}=n_2c_v(T_f-T_2)=\frac{ | + | <center><math>Q_\mathrm{2in}=n_2c_v(T_f-T_2)=\frac{p_{2f}V-pV}{\gamma-1}</math></center> |
donde la presión final de cada cámara cumple, por ser el volumen constante, | donde la presión final de cada cámara cumple, por ser el volumen constante, | ||
Revisión de 08:33 11 jun 2016
Contenido |
1 Enunciado
Un recipiente adiabático de 2 m³ está dividido en dos cámaras cúbicas del mismo tamaño, separadas por una pared inmóvil rellena de un aislante térmico. Las dos cámaras están llenas de aire seco. La de la izquierda contiene aire a 102 kPa y 600 K. El aire de la derecha está también a 102 kPa, pero a 300 K. Sin quitar la pared central se retira el aislante térmico que contiene, permitiendo que las dos cámaras entren en contacto térmico entre sí (no con el exterior)
- Determine la temperatura final de equilibrio y la cantidad de calor que pasa de una cámara a la otra.
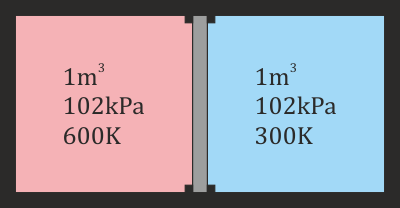
- Halle la fuerza sobre la pared central una vez que se ha alcanzado el equilibrio térmico.
Datos Constante universal de los gases ideales: 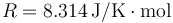 ; cociente entre capacidades caloríficas para el aire γ = 1.4.
; cociente entre capacidades caloríficas para el aire γ = 1.4.
2 Temperatura final
Vaya por delante que el problema se puede resolver de forma “mecánica” hallando el número de moles de cada gas y calculando luego la transferencia de calor, pero también puede resolverse de forma general sin emplear los moles.
Al ser el recipiente adiabático, todo el calor que sale de una de las cámaras entra en la otra
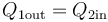
y, por ser los dos procesos a volumen constante y tratarse del mismo gas en ambas cámaras
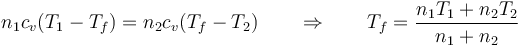
Puesto que inicialmente la presión es la misma en las dos cámaras, p, y también lo es su volumen, V, pero la temperatura de un gas (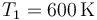 ) es el doble de la otra (
) es el doble de la otra (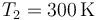 ) se deduce que el número de moles de una cámara es el doble de la otra
) se deduce que el número de moles de una cámara es el doble de la otra
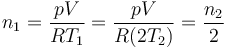
y por tanto, la temperatura final es
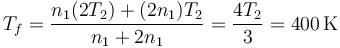
3 Calor transferido
La cantidad de calor que pasa de una cámara a la otra es
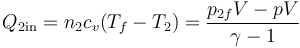
donde la presión final de cada cámara cumple, por ser el volumen constante,
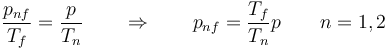
Esto nos da

y por tanto el calor
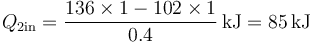
4 Fuerza sobre la pared
Puesto que conocemos la diferencia de presiones y el área de la pared (1m² por ser un cubo de 1m³ de volumen), la fuerza es inmediata