Ciclo Brayton
De Laplace
Contenido |
1 Enunciado
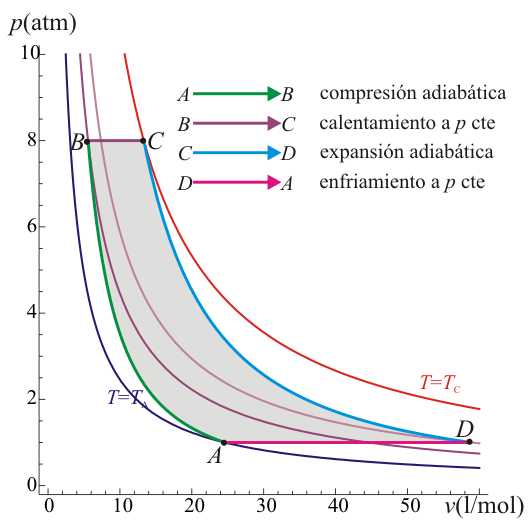
Un ciclo Brayton (o Joule) ideal modela el comportamiento de una turbina, como las empleadas en las aeronaves. Este ciclo está formado por cuatro pasos reversibles, según se indica en la figura. Pruebe que el rendimiento de este ciclo viene dado por la expresión
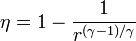
siendo r = pB / pA la relación de presión igual al cociente entre la presión al final del proceso de compresión y al inicio de él.. El método para obtener este resultado es análogo al empleado para el Ciclo Otto.
2 Descripción del ciclo
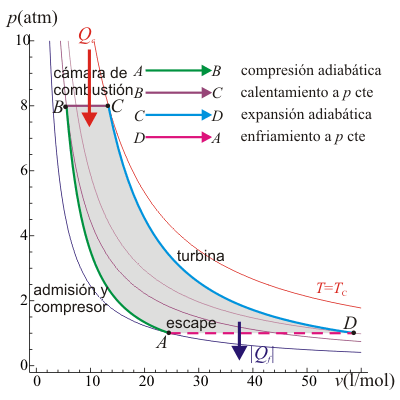
El ciclo Brayton describe el comportamiento ideal de un motor de turbina de gas, como los utilizados en las aeronaves. Las etapas del proceso son las siguientes:

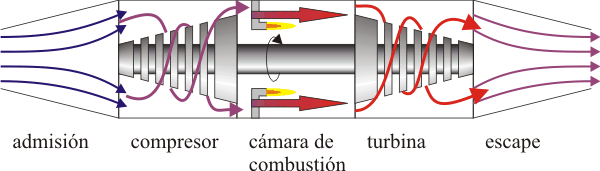
- Admisión
- El aire frío y a presión atmosférica entra por la boca de la turbina
- Compresor
- El aire es comprimido y dirigido hacia la cámara de combustión mediante un compresor (movido por la turbina). Puesto que esta fase es muy rápida, se modela mediante una compresión adiabática A→B.
- Cámara de combustión
- En la cámara, el aire es calentado por la combustión del queroseno. Puesto que la cámara está abierta el aire puede expandirse, por lo que el calentamiento se modela como un proceso isóbaro B→C.
- Turbina
- El aire caliente pasa por la turbina, a la cual mueve. En este paso el aire se expande y se enfría rápidamente, lo que se describe mediante una expansión adiabática C →D.
- Escape
- Por último, el aire enfriado (pero a una temperatura mayor que la inicial) sale al exterior. Técnicamente, este es un ciclo abierto ya que el aire que escapa no es el mismo que entra por la boca de la turbina, pero dado que sí entra en la misma cantidad y a la misma presión, se hace la aproximación de suponer una recirculación. En este modelo el aire de salida simplemente cede calor al ambiente y vuelve a entrar por la boca ya frío. En el diagrama PV esto corresponde a un enfriamiento a presión constante D→A.
Existen de hecho motores de turbina de gas en los que el fluido efectivamente recircula y solo el calor es cedido al ambiente. Para estos motores, el modelo del ciclo de Brayton ideal es más aproximado que para los de ciclo abierto.
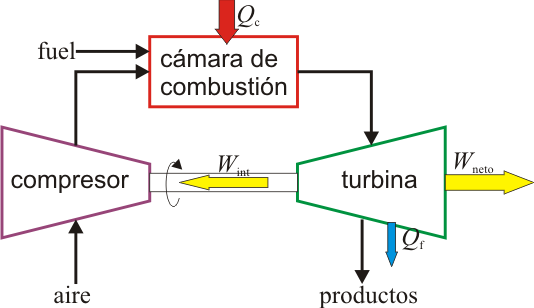
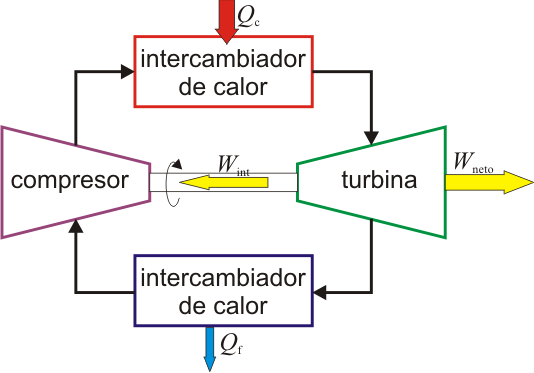
| 
|
| Motor de turbina de gas de ciclo abierto. | Motor de turbina de gas de ciclo cerrado. |
3 Eficiencia en función del calor
3.1 Intercambio de calor
De los cuatro procesos que forman el ciclo cerrado, no se intercambia calor en los procesos adiabáticos A→B y C→D, por definición. Sí se intercambia en los dos procesos isóbaros.
- En la combustión B→C, una cierta cantidad de calor Qc (procedente de la energía interna del combustible) se transfiere al aire. Dado que el proceso sucede a presión constante, el calor coincide con el aumento de la entalpía
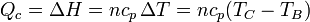
- El subíndice "c" viene de que este calor se intercambia con un supuesto foco caliente.
- En la expulsión de los gases D→A el aire sale a una temperatura mayor que a la entrada, liberando posteriormente un calor | Qf | al ambiente. En el modelo de sistema cerrado, en el que nos imaginamos que es el mismo aire el que se comprime una y otra vez en el motor, modelamos esto como que el calor | Qf | es liberado en el proceso D→A, por enfriamiento. El valor absoluto viene de que, siendo un calor que sale del sistema al ambiente, su signo es negativo. Su valor, análogamente al caso anterior, es
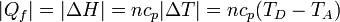
- El subíndice "f" viene de que este calor se cede a un foco frío, que es el ambiente.
3.2 Trabajo realizado
En este ciclo (a diferencia de lo que ocurre en el ciclo Otto) se realiza trabajo en los cuatro procesos. En dos de ellos el gtrabajo es positivo y en dos es negativo.
- En la compresión de la mezcla A→B, se realiza un trabajo positivo sobre el gas. Al ser un proceso adiabático, todo este trabajo se invierte en incrementar la energía interna, elevando su temperatura:
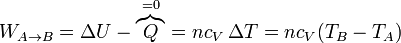
- En la combustión el gas se expande a presión constante, por lo que el trabajo es igual a la presión por el incremento de volumen, cambiado de signo:
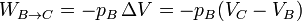
- Este trabajo es negativo, ya que es el aire, al expandirse, el que realiza el trabajo. Aplicando la ecuación de los gases ideales y que pB = pC, podemos escribir este trabajo como
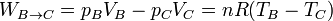
- En la expansión C→D es el aire el que realiza trabajo sobre el pistón. De nuevo este trabajo útil equivale a la variación de la energía interna
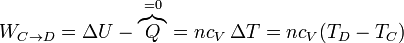
- este trabajo es negativo, por ser el sistema el que lo realiza.
- En el enfriamiento en el exterior tenemos una compresión a presión constante:
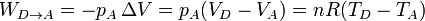
- El trabajo neto realizado sobre el gas es la suma de los cuatro términos
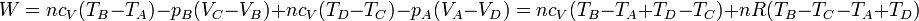
Aplicando la ley de Mayer
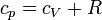
este trabajo se puede expresar como
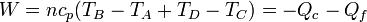
Por tratarse de un proceso cíclico, la variación de la energía interna es nula al finalizar el ciclo. Esto implica que el calor neto introducido en el sistema esigual al trabajo neto realizado por este, en valor absoluto.
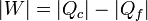
3.3 Rendimiento
El rendimiento (o eficiencia) de una máquina térmica se define, en general como “lo que sacamos dividido por lo que nos cuesta”. En este caso, lo que sacamos es el trabajo neto útil, | W | . Lo que nos cuesta es el calor Qc, que introducimos en la combustión. No podemos restarle el calor | Qf | ya que ese calor se cede al ambiente y no es reutilizado (lo que violaría el enunciado de Kelvin-Planck). Por tanto
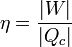
Sustituyendo el trabajo como diferencia de calores
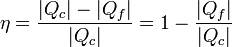
Esta es la expresión general del rendimiento de una máquina térmica.
4 Eficiencia en función de las temperaturas
Sustituyendo las expresiones del calor que entra en el sistema, | Qc | , y el que sale de él, | Qf | , obtenemos la expresión del rendimiento
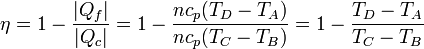
Vemos que el rendimiento no depende de la cantidad de aire que haya en la cámara, ya que n se cancela.
Podemos simplificar estas expresiones observando que B→C y D→A son procesos isóbaros, por lo que
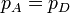
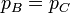
y que A→B y C→D son adiabáticos, por lo que cumplen la ley de Poisson (suponiéndolos reversibles)
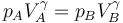
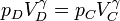
con γ = 1.4 la relación entre las capacidades caloríficas a presión constante y a volumen constante. Sustituyendo aquí la ecuación de los gases ideales V = nRT / p nos quedan las relaciones entre presiones y temperaturas
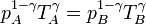
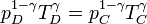
Sustituyendo la igualdad de presiones
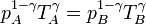
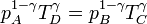
y dividiendo la segunda por la primera, obtenemos la igualdad de proporciones
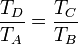
Restando la unidad a cada miembro
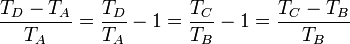
Intercambiando el denominador del primer miembro, con el numerador del último llegamos a
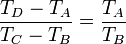
y obtenemos finalmente el rendimiento
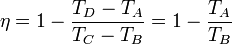
esto es, la eficiencia depende solamente de la temperatura al inicio y al final del proceso de compresión, y no de la temperatura tras la combustión, o de la cantidad de calor que introduce ésta.
Puesto que TB < TC, siendo TC la temperatura máxima que alcanza el aire, vemos ya que este ciclo va a tener un rendimiento menor que un ciclo de Carnot que opere entre esas las temperaturas TA y TC.
5 Eficiencia en función de la relación de presión
Aplicando de nuevo la relación de Poisson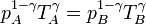
podemos expresar el rendimiento como
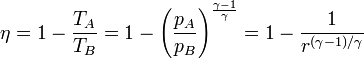
con r = pB / VA la relación de presión entre la presión final y la inicial.
La eficiencia teórica de un ciclo Brayton depende, por tanto, exclusivamente de la relación de presiones. Para un valor típico de 8 esta eficiencia es del 44.8%.
6 Caso práctico
Como caso concreto, consideraremos una central eléctrica de turbina de gas que opera en un ciclo Brayton ideal y tiene una relación de presión de 8. La temperatura del gas es de 300 K en la entrada del compresor y de 1300 K en la entrada de la turbina. Determinaremos la temperatura del gas a la salida del compresor y de la turbina, y la eficiencia de esta turbina.6.1 Eficiencia
La eficiencia de este ciclo es
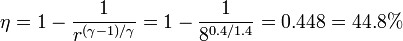
Esto quiere decir que más de la mitad del calor que entra en el ciclo ideal es disipada al exterior y solo un 45% es aprovechado como trabajo. En una turbina real la eficiencia es aun más baja.
6.2 Temperaturas
La temperatura a la salida del compresor, TB, puede calcularse empleando la ley de Poisson
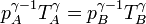
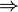
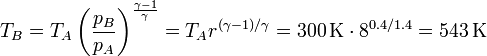
Vemos que la compresión incrementa la temperatura en 243 K, mientras que la combustión lo hace en (1300−543) K = 757 K, más del triple que la compresión.
Del mismo modo se calcula la temperatura a la salida de la turbina
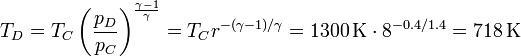
El gas a la salida está a una temperatura muy superior a la del ambiente, por lo que la entrega de calor al foco frío es muy importante.
7 Motores de reacción
El ciclo Brayton descrito aquí sirve para modelar el comportamiento de un motor de turbina que mueve una hélice, pero no para un motor a reacción.
La diferencia es que:
- En un avión de hélice interesa obtener el máximo trabajo neto que puede dar la turbina, para mover la hélice.
- En el motor a reacción, en cambio, interesa obtener el mínimo, que es el que mantiene en marcha el compresor (y resto de sistemas de la aeronave). El resto de la energía interna aprovechable no se extrae del gas, sino que se mantiene en él, en forma de energía cinética. La cantidad de movimiento que se llevan los gases expulsados es lo que impulsa al avión hacia adelante, de acuerdo con la tercera ley de Newton.
Puesto que el trabajo neto en un avión a reacción es cero, su eficiencia se define no por el trabajo realizado, sino por la potencia de propulsión dividida por el calor inyectado por unidad de tiempo.
8 Enlaces
- Artículo sobre el ciclo Brayton en el curso de Termodinámica del MIT.